Le henné, toujours en attente d’une réglementation !
Agent conditionneur, colorant capillaire,1 le henné est bien connu de l’inventaire européen. Cette poudre, obtenue à partir des feuilles séchées de Lawsonia inermis, fait partie de l’arsenal thérapeutique traditionnel de certains pays du monde. Utilisé pour traiter les brûlures2 ou d’autres pathologies, le henné est également largement employé à des fins d’embellissement pratiqués rituellement. En matière de réglementation, on évoque une limitation de la teneur en lawsone… à voir !
Un ingrédient qui possède une longue histoire
Dans le domaine cosmétique, le henné est employé depuis longtemps et c’est même trop peu que de le dire. Les femmes en utilisent depuis l’âge du bronze.3 Sur certaines fresques, telle celle figurant sur le mur de la Maison des dames d’Akrotiri, il est possible d’observer des femmes dont les mains, les pieds, les ongles sont ornés de graphismes réalisés au henné.4 En préparation de son mariage, une pâte de henné est appliquée sur la peau de la jeune fille ; des feuilles, des fleurs, des formes géométriques sont dessinées durant la cérémonie Mehndi.5
Un ingrédient de teinture capillaire
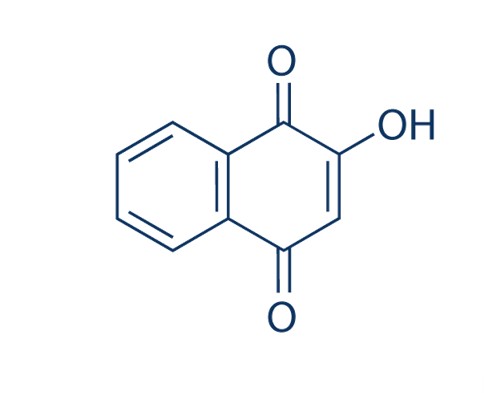
Le henné rouge est la feuille séchée et réduite en poudre de Lawsonia inermis. Quelques cas de dermatite de contact allergique causée par la lawsone ou 2-hydroxy-1,4-naphtoquinone (CI 75480, Natural Orange 6), l’un de ses constituants, ont été rapportés. L’allergie de type I est rare et constitue principalement un risque professionnel chez les coiffeurs ; les manifestations étant les suivantes : éternuements, conjonctivite, nez qui coule, toux sèche, dyspnée, gonflement du visage ou urticaire généralisée.6 Il faut faire attention à la qualité de la poudre utilisée, des traces de plomb étant détectées dans certains échantillons.7
Outre la lawsone, l’extrait de feuilles renferme des tanins, à caractère astringent.8 Pour le reste, on aimerait connaître avec précision la composition phytochimique de cet ingrédient à la composition complexe.
Un ingrédient qui peut se glisser dans les bains de bouche
En 2022, des équipes iraniennes se proposent de tester des bains de bouche à base de henné (extrait aqueux de henné à hauteur de 2 % solubilisé dans un mélange d’eau, d’alcool et de glycérine), dans le cadre du traitement d’une pathologie touchant la muqueuse buccale, le lichen plan oral. Entre le bain de bouche à la chlorhexidine et le bain de bouche au henné, on ne voit visiblement pas de différence.9
Un ingrédient qui peut se glisser dans les crèmes médicamenteuses
Il existe à ce jour peu de traitement efficace de la radiodermite, c’est pourquoi des équipes allemandes et iraniennes ont tenté de proposer une prise en charge possible à l’aide d’une crème au henné. Les tests réalisés sur des femmes atteintes de cancer du sein, traitées par radiothérapie, semblent montrer que des résultats similaires à ceux observés avec un corticoïde sont susceptibles d’être obtenus avec une crème à base de henné.10 Similaires ou supérieurs selon les produits de référence employés.11
En ce qui concerne le syndrome mains-pieds, lié à certaines chimiothérapies, il n’en va pas de même. Un essai réalisé à l’aide d’une pommade au henné et de curcumine ne s’est pas avéré positif en matière de service médical rendu.12
Un ingrédient dangereux en cas de favisme
Chez les sujets présentant un déficit enzymatique en G6PD (Glucose-6-Phosphate-Déshydrogénase), le henné peut induire une hémolyse par voie cutanée ou digestive.13-15 L’application traditionnelle de henné sur la peau des nouveau-nés s’est ainsi traduite, au fil, des ans, par un certain nombre d’hospitalisations, ayant fait l’objet de publications dans la littérature scientifique.16 Un décès est même à déplorer.17 Ceci est mis en lien avec le fait que la lawsone, contenue dans le henné, est un agent capable de provoquer une hémolyse (elle se comporte comme un puissant oxydant des hématies déficientes en G6PD).18,19
Un ingrédient modifié, adultéré
Dans un très grand nombre de cas, le henné utilisé pour le tatouage de la peau, contient de la paraphénylène-diamine (PPD), entre 0,4 et 30 % selon les échantillons et voire même plus, ce qui augmente considérablement le risque de dermatite de contact.20 On sait que dans les pays du Moyen-Orient, il est possible de trouver ce que les vendeurs locaux appellent « pierre de henné » ou « pierre allemande », une pierre présentée comme naturellement présente au niveau de la roche. Les dosages effectués avec ces pierres démontrent la supercherie… la PPD y étant présente à des teneurs de l’ordre de 85 à 90 %.21
Le henné par lui-même est peu sensibilisant.22
Sa couleur naturelle brun-orange est modifiée à l’aide de PPD par les tatoueurs, qui cherchent à intensifier sa couleur de cette façon.23
En 2020, une équipe allemande proposait de réaliser le rinçage de la peau avec une préparation à base de PEG-400, afin de pouvoir éliminer efficacement et simplement les tatouages au henné dit noir.24
Le henné, en bref
En ce qui concerne le henné (nom INCI : Lawsonia inermis extract), le CSSC assure une sécurité d’emploi, en tant que colorant capillaire, pour un henné renfermant au maximum 1,4 % de lawsone,25 ce qui semble en accord avec la composition de cette plante (teneur en lawsone dans les feuilles de 0,8 % (matière sèche)) à condition de réaliser, par exemple, une pâte avec 100 g de poudre de henné mélangée avec 300 mL d’eau bouillante.26 Pour autant cet ingrédient n’est pas réglementé à l’heure actuelle, malgré un effet mutagène/génotoxique possible.27,28 On attend une réglementation depuis l’âge du bronze, alors maintenant… on n’est plus très pressé… On attend !
Bibliographie
1 https://ec.europa.eu/growth/tools-databases/cosing/index.cfm?fuseaction=search.details_v2&id=34247
2 Mrabti HN, Doudach L, Mekkaoui M, Khalil Z, Harraqui K, Fozia F, Naceiri Mrabti N, El-Shazly M, Alotaibi A, Ullah R, Faouzi MEA, Bouyahya A. Profile of Medicinal Plants Traditionally Used for the Treatment of Skin Burns. Evid Based Complement Alternat Med. 2022 Jun 6;2022:3436665
3 Pradhan R, Dandawate P, Vyas A, Padhye S, Biersack B, Schobert R, Ahmad A, Sarkar FH. From body art to anticancer activities: perspectives on medicinal properties of henna. Curr Drug Targets. 2012 Dec;13(14):1777-98
4 Badoni Semwal R, Semwal DK, Combrinck S, Cartwright-Jones C, Viljoen A. Lawsonia inermis L. (henna): ethnobotanical, phytochemical and pharmacological aspects. J Ethnopharmacol. 2014 Aug 8;155(1):80-103
5 Wang MX, Maranda EL, Cortizo J, Lim V, Jimenez J. Henna–A Temporary Body of Art. JAMA Dermatol. 2016 Mar;152(3):290
6 Gavazzoni Dias MF. Hair cosmetics: an overview. Int J Trichology. 2015 Jan-Mar;7(1):2-15
7 Jallad KN, Espada-Jallad C. Lead exposure from the use of Lawsonia inermis (henna) in temporary paint-on-tattooing and hair dying. Sci Total Environ. 2008 Jul 1;397(1-3):244-50
8 Swan BC, Tam MM, Higgins CL, Nixon RL. Allergic contact dermatitis to substitute hair dyes in a patient allergic to para-phenylenediamine: Pure henna, black tea and indigo powder. Australas J Dermatol. 2016 Aug;57(3):219-21
9 Kakoei S, Karbasi N, Raeiszadeh M, Tajadini H, Nekouei AH. The efficacy of henna (Lawsonia inermis L.) mouthwash versus chlorhexidine gluconate 0.2% mouthwash as adjuvant therapy of oral lichen planus: A randomized double-blind clinical trial. J Ethnopharmacol. 2022 May 23;290:115037
10 Pasalar M, Ahadi B, Mirzaei HR, Buentzel J, Mehri Ardestani M, Kamian S, Heydarirad G. Comparing Dermolina-Henna Cream with Mometasone Cream in Improving Radiodermatitis Among Patients with Breast Cancer: A Randomized Active-Control Double-Blind Clinical Trial. J Integr Complement Med. 2022 Nov;28(11):895-903
11 Ansari M, Farzin D, Mosalaei A, Omidvari S, Ahmadloo N, Mohammadianpanah M. Efficacy of topical alpha ointment (containing natural henna) compared to topical hydrocortisone (1%) in the healing of radiation-induced dermatitis in patients with breast cancer: a randomized controlled clinical trial. Iran J Med Sci. 2013 Dec;38(4):293-300
12 Elyasi S, Rasta S, Taghizadeh-Kermani A, Hosseini S. Topical henna and curcumin (Alpha®) ointment efficacy for prevention of capecitabine induced hand-foot syndrome: A randomized, triple-blinded, placebo-controlled clinical. Daru. 2022 Jun;30(1):117-125
13 Anilkumar S. Henna. Heart Views. 2021 Jan-Mar;22(1):79
14 Yildizhan E, Aslan Sirakaya H, Korkmaz S. Therapeutic plasma exchange in non-immune hemolytic anemia associated with henna ingestion: A case report. Transfus Apher Sci. 2021 Dec;60(6):103204
15 Kök AN, Ertekin MV, Ertekin V, Avci B. Henna (Lawsonia inermis Linn.) induced haemolytic anaemia in siblings. Int J Clin Pract. 2004 May;58(5):530-2
16 Kandil HH, al-Ghanem MM, Sarwat MA, al-Thallab FS. Henna (Lawsonia inermis Linn.) inducing haemolysis among G6PD-deficient newborns. A new clinical observation. Ann Trop Paediatr. 1996 Dec;16(4):287-91
17 Lee SW, Lai NM, Chaiyakunapruk N, Chong DW. Adverse effects of herbal or dietary supplements in G6PD deficiency: a systematic review. Br J Clin Pharmacol. 2017 Jan;83(1):172-179
19 Zinkham WH, Oski FA. Henna: a potential cause of oxidative hemolysis and neonatal hyperbilirubinemia. Pediatrics. 1996 May;97(5):707-9
20 Al-Suwaidi A, Ahmed H. Determination of para-phenylenediamine (PPD) in henna in the United Arab Emirates. Int J Environ Res Public Health. 2010 Apr;7(4):1681-93
21 Özkaya E, Yazganoglu KD, Arda A, Topkarci Z, Erçag E. The « henna stone » myth. Indian J Dermatol Venereol Leprol. 2013 Mar-Apr;79(2):254-6
22 Kazandjieva J, Grozdev I, Tsankov N. Temporary henna tattoos. Clin Dermatol. 2007 Jul-Aug;25(4):383-7
23 Kluger N, Raison-Peyron N, Guillot B. Tatouages temporaires au henné : des effets indésirables parfois graves. Presse Med. 2008 Jul-Aug;37(7-8):1138-42
24 Ferrari DM, Hoffmann JC, Schön MP, Lippert U. Efficient removal of black henna tattoos. Pediatr Dermatol. 2020 Nov;37(6):1063-1067
25 https://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_140.pdf
26 Charoensup R, Duangyod T, Palanuvej C, Ruangrungsi N. Pharmacognostic Specifications and Lawsone Content of Lawsonia inermis Leaves. Pharmacognosy Res. 2017 Jan-Mar;9(1):60-64
27 https://ec.europa.eu/health/ph_risk/committees/sccp/documents/out254_en.pdf
28 https://ec.europa.eu/growth/tools-databases/cosing/index.cfm?fuseaction=search.details_v2&id=34993