L’acide fulvique, ne faisons pas entrer le fauve dans la cage cosmétique !
Obtenu par fermentation microbienne de la paille ou du fumier de bétail,1 constituant de la tourbe,2 de la bouse de vache compostée,3 l’acide fulvique fleure bon la nature, la décomposition. Cet engrais naturel, qui permet d’obtenir des pivoines de compétition, même dans des milieux pauvres en eau,4 a commencé à livrer quelques-uns de ses secrets au début du XXe siècle. Et à l’heure actuelle, cet acide entre dans la composition de quelques cosmétiques. Cosmetikwatch s’en fait l’écho dans une de ses newsletters, présentant cet ingrédient comme un actif très peu utilisé, mais toutefois susceptible d’être croisé dans une brume au nom transparent « Fulvic acid »5 ou bien dans un produit nettoyant au nom tout aussi transparent (Fulvic acid cleanser).6
Extraire un actif de la tourbe, valoriser du compost… que ces mots sonnent bien à l’oreille de celles et ceux qui souhaitent employer le terme de « up-cycling » dans leur argumentaire marketing.
Il y a un hic, toutefois, il va falloir être prudent quant à l’exploitation de ce déchet qui ne coûte rien et semble pouvoir permettre de rapporter gros. Il va falloir se pencher sur son profil toxicologique et assurer une pureté optimale à un ingrédient à la composition pour le moins fluctuante !
L’acide fulvique, son histoire
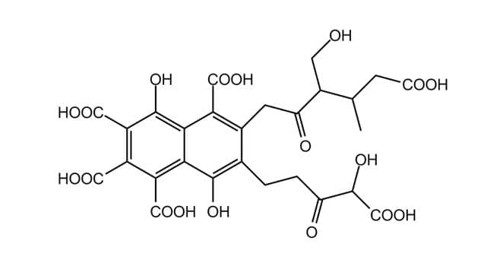
Son histoire commence dans un laboratoire de biochimie londonien. Trois chercheurs Albert Oxford, Harold Raistrick et Paul Simonart travaillent, dans les années 1930, sur des cultures de Penicillium griseolfulvum. Ces chercheurs facétieux s’amusent alors à modifier la composition du milieu de culture de cette moisissure, afin de voir quelles en seront les conséquences d’un point de vue métabolique. Ils se rendent compte que lorsque ce champignon est placé dans un milieu où la seule source de carbone est le glucose et la seule source d’azote le nitrate de sodium il est possible d’identifier dans le milieu de culture quatre molécules, l’acide 6 méthyl salicylique, l’acide gentisique, l’acide fumarique et le mannitol. En revanche, lorsque l’on utilise comme substrat pour le Penicillium non plus des ions nitrate (NO3-) mais des ions ammonium (NH4+), ce n’est pas du tout la même chanson ; en lieu et place des deux substances phénoliques incolores produites précédemment, on découvre une substance de couleur jaune et de formule brute : C14H12O8. Une substance jaune à laquelle les chercheurs donnent tout naturellement le nom d’acide fulvique (d’un point de vue étymologique, ce terme vient du latin « fulvus » désignant la couleur jaune). Les chercheurs constatent, toutefois, que le rendement de production est faible et que la molécule est difficile à isoler.7 Pour l’instant, de toute façon, on ne sait pas trop à quoi va bien pouvoir servir cette molécule ! Ce n’est pas comme la griséofulvine, promise à un bel avenir !8
Tout est clair (ou presque), on a obtenu ici une molécule dont on nous livre la formule brute ! La suite va se corser !
L’acide fulvique, une ambiguïté chimique
Présenté parfois comme une molécule, l’acide fulvique est également désigné, par certains auteurs, sous le nom de « fraction humique », retrouvée naturellement dans l’eau et la tourbe. Une fraction humique, qui provient de la décomposition de matériels végétaux et animaux par les microorganismes du sol. Dans ce cas-là, on n’évoque pas une molécule pure, mais un mélange de molécules possédant des fonctions carboxyliques, carbonyles, hydroxyles, phénoliques, quinones… ce qui explique sans doute que l’on attribue à cet acide fulvique un poids moléculaire fluctuant entre 500 et 5000 Daltons.9 Des analystes nous précisent que certaines tourbes peuvent fournir un acide fulvique composé de… 18 fractions isolées par HPLC.10 Des fractions dont la nature varie selon la composition du milieu entré en fermentation.11
Il est bon aussi de signaler que cet acide fulvique est un agent chélatant, susceptible de complexer un certain nombre de métaux,12 ce qui doit être pris en compte si l’on a à l’esprit l’idée de l’utiliser dans le domaine cosmétique !
En effet, d’une molécule purifiée… on est rendu à un ensemble de molécules de nature organique et inorganique. Une sorte de magma, dont la composition varie selon toutes sortes de critères, puisque les germes en présence (ceux-ci sont variables) vont décomposer différemment des matériaux végétaux et animaux qui sont forcément différents selon les zones géographiques, les saisons…
L’acide fulvique, une ambiguïté en matière d’innocuité
Il est à préciser que la consommation d’une eau trop riche en acide fulvique entraîne une pathologie, la maladie de Kashin-Beck ;13 il s’agit d’une arthropathie endémique en Chine. Des études réalisées sur des patients ont permis de mettre en évidence une altération du cartilage articulaire, liée à une modification de la structure du collagène II le composant. On observe également des problèmes de fragilité cutanée.14 Cela mérite donc réflexion.
Et pourtant, on ne compte plus, sur la toile, le nombre de publicités vantant les mérites de compléments alimentaires à base d’acide fulvique ! non merci. Pas pour nous !
L’acide fulvique, son activité thérapeutique dans le cadre de la dermatite atopique
Dans le cadre de la dermatite atopique (DA), des tests in vitro et sur modèle animal montrent le caractère anti-inflammatoire de cette molécule (ou plutôt de cet ensemble de molécules) et ouvrent des portes en matière de traitement de cette pathologie.15
Un essai clinique de phase 1, réalisé en Afrique du Sud, avait été, dans le sens, en 2012, de l’innocuité et de l’efficacité de la prise orale d’acide fulvique dans le cadre du traitement de la dermatite atopique. La posologie était de 40 mL d’une préparation dosée à 3,8 % d’acide fulvique, 2 fois par jour, pendant une semaine.9 Depuis, pas de nouvelles.
L’acide fulvique, son activité thérapeutique dans le cadre de plaies
Le caractère anti-inflammatoire et antiradicalaire de cet ingrédient explique son caractère cicatrisant. Sur modèle animal, on observe de bons résultats pour un cataplasme dosé à 0,5 % en acide fulvique.16
L’acide fulvique, son activité thérapeutique, dans le cadre de l’hygiène bucco-dentaire
Du fait de son efficacité vis-à-vis de l’effet inhibiteur de la croissance de Porphyromonas gingivalis, certains auteurs envisageaient en 2013 de mettre au point des bains de bouche permettant de traiter les parodontopathies.17
L’acide fulvique, un additif thérapeutique
Lorsque l’acide fulvique n’est pas présenté comme un principe actif, il nous est vendu comme un additif susceptible d’améliorer la solubilité et l’absorption cutanée de certains principes actifs, comme la thymoquinone, par exemple. Difficile de savoir le rôle exact joué spécifiquement par l’acide fulvique, lorsque l’on voit que l’émulsion testée est composée de tensioactifs comme le Tween®80 et le Transcutol®P.18,19
L’acide fulvique, son activité en matière environnementale
On constate que cette molécule, en tant que piégeur de radicaux libres, permet d’inhiber le photovieillissement des matières plastiques, dans l’environnement. C’est du moins ce qui est observé dans le cas du polypropylène, qui se dégrade plus facilement dans une eau pure en laboratoire que dans l’eau d’un lac contenant de l’acide humique et de l’acide fulvique.20 Cet avis n’est pas partagé par tous, puisque d’autres auteurs considèrent, au contraire, que l’acide fulvique favorise la photodégradation du polypropylène.21 A creuser, donc…
Comme on constate une augmentation de la concentration des substances humiques dans les milieux aquatiques, des chercheurs tchèques, allemands et chinois se sont posé la question de savoir quelle serait l’influence de l’acide fulvique sur la truite arc-en-ciel. On constate, effectivement, un impact sur le système immunitaire de ce poisson, avec une augmentation notoire (augmentation de 77 %) des immunoglobulines présentes au niveau cutané. Le mucus produit s’avère par conséquent plus efficace en matière de lutte contre certains genres bactériens.22
Le poisson-zèbre, quant à lui, préfère nettement les microplastiques de polyamide non traités par l’acide fulvique, par rapport à ceux qui ont subi un phénomène de photovieillissement catalysé par lui.23
Pour le concombre de mer (Apostichopus japonicas), la présence d’acide fulvique dans son alimentation ne lui fait… ni chaud ni froid.24
Pour l’inventaire européen
Pas d’épanchement sur la monographie de l’acide fulvique, qui nous est présenté comme un « conditionneur cutané »… sans plus de détails.25 Le n°CAS annoncé (CAS 479-66-3) nous envoie à des fiches techniques d’une molécule dont la formule brute ne nous est pas inconnue (voir à ce sujet le paragraphe 2).26
L’acide fulvique, en bref
Cet ingrédient, qui peut être présenté comme vertueux, éco-responsable, green, acteur de l’économie circulaire, pose plus de questions qu’il n’apporte de réponses. On ne sait pas trop bien ce qui est employé par les sociétés qui l’utilisent. Un extrait de tourbe ? de compost de pailles ? de bouses de vaches ? Un extrait, à la composition complexe et parfois assez douteuse ou bien, au contraire une molécule extrêmement pure. Quid de la toxicologie de cet ingrédient ? Quid de son intérêt cosmétique ? Beaucoup de points d’interrogation qui devront trouver réponses, avant que nous nous mettions à nous tartiner la peau avec des préparations en contenant.
Un peu trop sauvage, un peu trop fauve, à notre goût, cet acide fulvique !
Bibliographie
1 Li J, Nie Z, Fan Z, Li C, Liu B, Hua Q, Hou C. Biochemical Fulvic Acid Modification for Phosphate Crystal Inhibition in Water and Fertilizer Integration. Materials (Basel). 2022 Feb 3;15(3):1174
2 Jarukas L, Ivanauskas L, Kasparaviciene G, Baranauskaite J, Marksa M, Bernatoniene J. Determination of Organic Compounds, Fulvic Acid, Humic Acid, and Humin in Peat and Sapropel Alkaline Extracts. Molecules. 2021 May 18;26(10):2995
3 Ran S, He T, Zhou X, Yin D. Effects of fulvic acid and humic acid from different sources on Hg methylation in soil and accumulation in rice. J Environ Sci (China). 2022 Sep;119:93-105
4 Fang Z, Wang X, Zhang X, Zhao D, Tao J. Effects of fulvic acid on the photosynthetic and physiological characteristics of Paeonia ostii under drought stress. Plant Signal Behav. 2020 Jul 2;15(7):1774714
5 https://en.oiolab.co/products/fulvic-ionic
7 Oxford AE, Raistrick H, Simonart P. Studies in the biochemistry of micro-organisms: Fulvic acid, a new crystalline yellow pigment, a metabolic product of P. griseo-fulvum Dierckx, P. flexuosum Dale and P. Brefeldianum Dodge. Biochem J. 1935 May;29(5):1102-15
8 Oxford AE, Raistrick H, Simonart P. Studies in the biochemistry of micro-organisms: Griseofulvin, C(17)H(17)O(6)Cl, a metabolic product of Penicillium griseo-fulvum Dierckx. Biochem J. 1939 Feb;33(2):240-8
9 Gandy JJ, Meeding JP, Snyman JR, van Rensburg CE. Phase 1 clinical study of the acute and subacute safety and proof-of-concept efficacy of carbohydrate-derived fulvic acid. Clin Pharmacol. 2012;4:7-11
10 Beer AM, Junginger HE, Lukanov J, Sagorchev P. Evaluation of the permeation of peat substances through human skin in vitro. Int J Pharm. 2003 Mar 6;253(1-2):169-75
11 Wu D, Lu Y, Ma L, Cheng J, Wang X. Preparation and Molecular Structural Characterization of Fulvic Acid Extracted from Different Types of Peat. Molecules. 2023 Sep 23;28(19):6780
12 Song C, Sun S, Wang J, Gao Y, Yu G, Li Y, Liu Z, Zhang W, Zhou L. Applying fulvic acid for sediment metals remediation: Mechanism, factors, and prospect. Front Microbiol. 2023 Jan 9;13:1084097
13 Yang C, Niu C, Bodo M, Gabriel E, Notbohm H, Wolf E, Müller PK. Fulvic acid supplementation and selenium deficiency disturb the structural integrity of mouse skeletal tissue. An animal model to study the molecular defects of Kashin-Beck disease. Biochem J. 1993 Feb 1;289 ( Pt 3)(Pt 3):829-35
14 Yang CL, Bodo M, Notbohm H, Peng A, Müller PK. Fulvic acid disturbs processing of procollagen II in articular cartilage of embryonic chicken and may also cause Kashin-Beck disease. Eur J Biochem. 1991 Dec 18;202(3):1141-6
15 Wu C, Lyu A, Shan S. Fulvic Acid Attenuates Atopic Dermatitis by Downregulating CCL17/22. Molecules. 2023 Apr 16;28(8):3507
16 Samiee-Rad F, Hosseini Sedighi SF, Taherkhani A, Gheibi N. Evaluation of Healing Effects of Poultice Containing 0.5% Fulvic Acid on Male White-Male Rats with Skin Ulcer. J Cutan Aesthet Surg. 2022 Jan-Mar;15(1):40-47
17 Sherry L, Millhouse E, Lappin DF, Murray C, Culshaw S, Nile CJ, Ramage G. Investigating the biological properties of carbohydrate derived fulvic acid (CHD-FA) as a potential novel therapy for the management of oral biofilm infections. BMC Oral Health. 2013 Sep 24;13:47
18 Khan R, Mirza MA, Aqil M, Hassan N, Zakir F, Ansari MJJ, Iqbal Z. A Pharmaco-Technical Investigation of Thymoquinone and Peat-Sourced Fulvic Acid Nanoemulgel: A Combination Therapy. Gels. 2022 Nov 10;8(11):733
19 Khan R, Mirza MA, Aqil M, Alex TS, Raj N, Manzoor N, Naseef PP, Saheer Kuruniyan M, Iqbal Z. In Vitro and In Vivo Investigation of a Dual-Targeted Nanoemulsion Gel for the Amelioration of Psoriasis. Gels. 2023 Jan 28;9(2):112
20 Wu X, Liu P, Gong Z, Wang H, Huang H, Shi Y, Zhao X, Gao S. Humic Acid and Fulvic Acid Hinder Long-Term Weathering of Microplastics in Lake Water. Environ Sci Technol. 2021 Dec 7;55(23):15810-15820
21 Cao R, Liu X, Duan J, Gao B, He X, Nanthi Bolan, Li Y. Opposite impact of DOM on ROS generation and photoaging of aromatic and aliphatic nano- and micro-plastic particles. Environ Pollut. 2022 Dec 15;315:120304
22 Lieke T, Stejskal V, Behrens S, Steinberg CEW, Meinelt T. Fulvic acid modulates mucosal immunity in fish skin: Sustainable aquaculture solution or environmental risk factor? J Hazard Mater. 2024 Apr 5;467:133737
23 Zhang X, Xia M, Zhao J, Cao Z, Zou W, Zhou Q. Photoaging enhanced the adverse effects of polyamide microplastics on the growth, intestinal health, and lipid absorption in developing zebrafish. Environ Int. 2022 Jan;158:106922
24 Dou H, Wu S. Dietary fulvic acid supplementation improves the growth performance and immune response of sea cucumber (Apostichopus japonicas). Fish Shellfish Immunol. 2023 Apr;135:108662
25 https://ec.europa.eu/growth/tools-databases/cosing/details/87166
26 https://www.scbt.com/fr/p/fulvic-acid-479-66-3