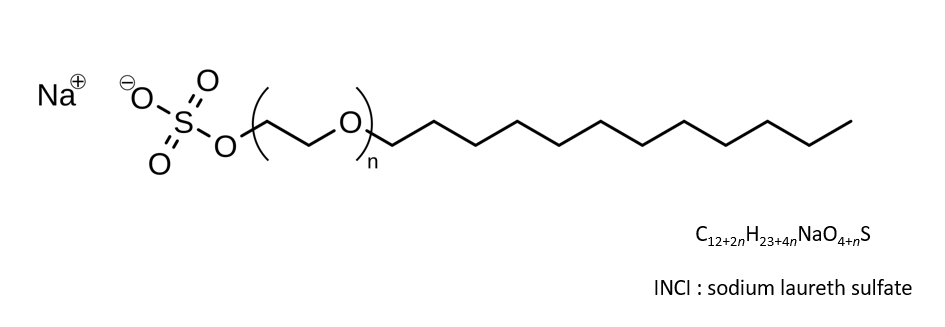
Le lauryléthersulfate de sodium, il est partout, on vous dit tout !
Le lauryléthersulfate de sodium (INCI : sodium laureth sulfate) est un tensioactif anionique, très bon moussant,1 très largement employé dans le domaine cosmétique, aussi bien pour l’hygiène de la peau que des cheveux,2 comme en témoignent les teneurs retrouvées dans les eaux usées.3
Un tensioactif que l’on retrouve partout et qu’il est donc bon de connaître… beaucoup !
Un tensioactif « pétrochimique » ?
Peu coûteux, issu de la pétrochimie, ce tensioactif, assez bien toléré, est boudé par certaines sociétés qui tendent à utiliser des tensioactifs dits « biosourcés », c’est-à-dire obtenus à partir d’ingrédients non pétrolifères.4
D’un point de vue chimique, il s’agit du sel de sodium de l’alcool laurique sulfaté et éthoxylé.5 Selon le degré d’éthoxylation, la nomenclature INCI différencie le sodium laureth-12 sulfate,6 du sodium laureth-8 sulfate7 ou du sodium laureth-40 sulfate8…
Un tensioactif « green » ?
Ce tensioactif peut également être obtenu à partir d’huiles végétales comme l’huile de coco ou de palme, ce qui explique, sans doute, pourquoi certains auteurs le qualifient de « green ». Toutefois, lorsque ces auteurs souhaitent l’associer à un lubrifiant perfluoré pour mettre au point des shampooings, on dit… non !9 Et quand on sait en plus que ce composé est un composé éthoxylé, on sourit un peu en lisant la mention « green » !
Un tensioactif hypertendu ?
Du moins un tensioactif qui ne boude pas les plaisirs salés. On sait que le chlorure de sodium joue le rôle de facteur épaississant en présence de ce tensioactif anionique. On sait que des ratios très précis de tensioactif et de sel sont nécessaires pour atteindre la viscosité voulue. Une publication américaine de 2019 nous donne les valeurs chiffrées d’un bon trinôme de produit nettoyant. La viscosité maximale du mélange de tensioactifs composé de lauryléthersulfate de sodium, de cocamidopropylbétaïne et de rhamnolipides (respectivement 10 % en poids, 2 % en poids et 4 % en poids) a été observée lorsque la concentration en chlorure de sodium était de 4 % en poids. Il est donc important de s’intéresser à ces ratios, afin de pouvoir exploiter au mieux les propriétés viscosantes du sel,10 un ingrédient bon marché !
Un effet désinfectant ?
C’est ce que l’on apprend en lisant cette publication de 2021 qui présente le lauryléthersulfate de sodium comme un adjuvant intéressant pour la désinfection des matériels contaminés par des levures comme Saccharomyces cerevisia, en association avec l’utilisation de la technique de l’eau activée par plasma.11
Un effet nettoyant ?
C’est peut-être une évidence, mais encore est-il bon de le préciser. Ce tensioactif est un bon agent nettoyant, qui permet, entre autres, d’éliminer le sébum, qui est présent en grande quantité chez le sujet à peau grasse. Une étude de 2019 nous dit, toutefois, qu’il vaut mieux utiliser un autre tensioactif comme le cocoylglutamate disodique, si l’on veut éviter d’observer un effet rebond en cas d’arrêt d’utilisation du produit.12
Un effet irritant ?
En matière de détermination d’un effet irritant au niveau cutané, deux éléments sont à prendre en compte : la durée d’application (ou temps de contact) et la concentration en irritant dans la préparation testée. Une étude publiée en 2003 nous permet ainsi de classer 3 tensioactifs en matière d’effet irritant. Le laurylsulfate de sodium s’avère le plus irritant de tous, comme on pouvait facilement s’y attendre. Vient ensuite le lauryléthersulfate de sodium (moins irritant) et l’alkylpolyglucoside (pas irritant). Afin d’établir ce classement, des patchs tests ont été réalisés sur un échantillon de 20 personnes, âgées de 18 à 60 ans (12 femmes et 8 hommes). Des solutions aqueuses diluées de ces tensioactifs (à des doses variant entre 0,125 et 2 %) ont été laissées au contact de la peau, pendant des temps variables (6 h, 12 h ou au pire 24 heures). La détermination de la perte insensible en eau témoin, lorsque cette valeur augmente, de l’altération de l’effet barrière de la peau a alors permis de se faire une idée sur la plus ou moins bonne tolérance des tensioactifs étudiés. On se rend compte, sans surprise, que la perte insensible en eau (PIE en g/h/m2) est d’autant plus importante que le tensioactif est employé à concentration élevée et qu’il reste (cerise sur le gâteau) un temps prolongé sur la peau. Concrètement, si on se place dans le pire des cas (solution la plus concentrée, soit 2 % et temps de contact le plus prolongé, soit 24 heures), on obtient une PIE de 40 g/h/m2 pour la solution de laurylsulfate de sodium, de 25 g/h/m2 pour le lauryléthersulfate de sodium et de 5 g/h/m2 pour le polyalkylglucoside, sachant que cette valeur de 5 correspond à la valeur physiologique (cas d’une peau normale). Si on s’intéresse au caractère durable de cette altération de la barrière cutanée, on se rend compte que le laurylsulfate de sodium provoque l’effet perturbateur de la fonction barrière le plus durable (effet sur 10 jours) ; il est suivi par le lauryléthersulfate de sodium (effet sur 3 jours) ; le polyalkylglucoside, qui n’est pas irritant, ne nécessite pas, quant à lui, de temps de régénération.13 On remarquera que, pour ce test, on utilise de faibles doses de tensioactif, en occlusif, sur une longue période, afin de pouvoir extrapoler ce qui se passe au quotidien, lorsque l’on utilise un produit d’hygiène fortement dosé en tensioactifs (la base lavante représente 30 % de la formule), avec un temps de contact limité, ces produits étant rincés.
On nous dira, tout de même, que ces patchs tests ne permettent pas de prédire ce qui se passe « dans la vraie vie », lorsque l’on rince le produit contenant ces tensioactifs… On répondra que ces tests sont prédictifs, puisque, lorsque l’on pratique un test d’usage (utilisation des produits en conditions réelles), on est capable de faire la différence entre des produits renfermant du laurylsulfate de sodium, un irritant notoire et ceux formulés avec du lauryléthersulfate de sodium,14 nettement moins irritant.
On a donc bien compris que tous les tensioactifs ne se valent pas en matière de conséquences sur la structure de la barrière cutanée. On sait, en outre, que plus le tensioactif est utilisé à concentration élevée, plus l’effet irritant observé sera important. Ceci explique pourquoi on n’hésitera pas à associer plusieurs tensioactifs entre eux dans les produits du commerce, afin de permettre l’obtention d’un produit que l’on qualifiera de « doux ».15 Et on évite les associations qui fâchent… le cocamide DEA (stabilisateur de mousse), à caractère irritant, étant susceptible de renforcer celui du lauryléthersulfate de sodium.16
Un effet pénétrant ?
On sait que le laurylsulfate de sodium et le lauryléthersulfate de sodium sont capables de pénétrer dans les couches profondes du Stratum corneum, plus facilement, en tout cas, qu’un polyalkylglucoside, car les micelles qu’ils forment dans l’eau sont de plus petites tailles.17 Cet effet « pénétrant » a pour conséquence la désorganisation des lipides intercellulaires, ce qui impacte l’état d’hydratation de la peau.18 Enfin, cet effet pénétrant est plus important chez le sujet atopique (dont la fonction barrière cutanée est altérée) que chez le sujet à peau normale.19
Rappelons que cet effet exhausteur de pénétration du lauryléthersulfate de sodium est connu de la littérature médicale, qui considère cet ingrédient comme un allié potentiel en cas de nécessité de forcer le passage cutané de principes actifs récalcitrants.20
En tout cas, un tensioactif « sulfaté »
Un tensioactif « sulfaté », dont la fonction sulfate, on ne sait pourquoi, est critiquée. De ce fait, on trouve des publications dans la littérature scientifique qui visent à associer des tensioactifs entre eux (alkyloléfine sulfonate, alkylpolyglucoside et laurylhydroxysultaïne), afin d’obtenir des produits d’hygiène aux qualités identiques à celles obtenues avec le binôme classique : lauryléthersulfate de sodium–cocamidopropylbétaïne.21
Le lauryléthersulfate de sodium, en bref
Il est à privilégier par rapport au laurylsulfate de sodium. Il convient à la majorité de la population. Toutefois, lorsque l’on veut formuler un produit nettoyant vraiment doux, il peut être bon d’aller chercher des tensioactifs encore moins irritants, voire pas irritants du tout !
Bibliographie
1 Jun S, Pelot DD, Yarin AL. Foam consolidation and drainage. Langmuir. 2012 Mar 27;28(12):5323-30
2 Ziółkowska D, Syrotynska I, Shyichuk A, Lamkiewicz J. Determination of SLES in Personal Care Products by Colloid Titration with Light Reflection Measurements. Molecules. 2021 May 5;26(9):2716
3 Brunning H, Sallach JB, Boxall A. Emissions of water-soluble polymers from household products to the environment: a prioritization study. Environ Toxicol Chem. 2025 Feb 1;44(2):563-588
4 Jansen LM, den Bakker PC, Venbrux N, van Rijbroek KWM, Klaassen-Heshof DJ, Lenferink WB, Lücker S, Ranoux A, Raaijmakers HWC, Boltje TJ. Synthesis and Performance of Bio-Based Amphoteric Surfactants. Chemistry. 2024 Jul 5;30(38):e202400986
5 https://ec.europa.eu/growth/tools-databases/cosing/details/79583
6 https://ec.europa.eu/growth/tools-databases/cosing/details/79585
7 https://ec.europa.eu/growth/tools-databases/cosing/details/79675
8 https://ec.europa.eu/growth/tools-databases/cosing/details/59269
9 Zhang D, Zhang Y, Bai Y, Tai X, Wang W, Wang G. Preparation and Property of Perfluoropolyether Emulsions. Polymers (Basel). 2019 May 29;11(6):932
10 Xu L, Amin S. Microrheological study of ternary surfactant-biosurfactant mixtures. Int J Cosmet Sci. 2019 Aug;41(4):364-370
11 Liu X, Li Y, Zhang R, Huangfu L, Du G, Xiang Q. Inactivation effects and mechanisms of plasma-activated water combined with sodium laureth sulfate (SLES) against Saccharomyces cerevisiae. Appl Microbiol Biotechnol. 2021 Apr;105(7):2855-2865
12 Weber N, Schwabe K, Schempp CM, Wölfle U. Effect of a botanical cleansing lotion on skin sebum and erythema of the face: A randomized controlled blinded half-side comparison. J Cosmet Dermatol. 2019 Jun;18(3):821-826
13 Löffler H, Happle R. Profile of irritant patch testing with detergents: sodium lauryl sulfate, sodium laureth sulfate and alkyl polyglucoside. Contact Dermatitis. 2003 Jan;48(1):26-32
14 Charbonnier V, Morrison BM Jr, Paye M, Maibach HI. Subclinical, non-erythematous irritation with an open assay model (washing): sodium lauryl sulfate (SLS) versus sodium laureth sulfate (SLES). Food Chem Toxicol. 2001 Mar;39(3):279-86
15 Takagi Y, Shimizu M, Morokuma Y, Miyaki M, Kiba A, Matsuo K, Isoda K, Mizutani H. A new formula for a mild body cleanser: sodium laureth sulphate supplemented with sodium laureth carboxylate and lauryl glucoside. Int J Cosmet Sci. 2014 Aug;36(4):305-11
16 Turkoglu M, Pekmezci E, Sakr A. Evaulation of irritation potential of surfactant mixtures. Int J Cosmet Sci. 1999 Dec;21(6):371-82
17 Hoppel M, Holper E, Baurecht D, Valenta C. Monitoring the distribution of surfactants in the stratum corneum by combined ATR-FTIR and tape-stripping experiments. Skin Pharmacol Physiol. 2015;28(3):167-75
18 Hoppel M, Baurecht D, Holper E, Mahrhauser D, Valenta C. Validation of the combined ATR-FTIR/tape stripping technique for monitoring the distribution of surfactants in the stratum corneum. Int J Pharm. 2014 Sep 10;472(1-2):88-93
19 Jung IK, Choi J, Nam J, No KT. Modeling lipid layers of atopic skin and observation of changes in lipid layer properties with changes in ceramide content. J Cosmet Dermatol. 2021 Sep;20(9):2924-2931
20 Karande P, Jain A, Mitragotri S. Discovery of transdermal penetration enhancers by high-throughput screening. Nat Biotechnol. 2004 Feb;22(2):192-7
21 Yorke K, Potanin A, Jogun S, Morgan A, Shen H, Amin S. High-performance sulphate-free cleansers: Surface activity, foaming and rheology. Int J Cosmet Sci. 2021 Dec;43(6):636-652