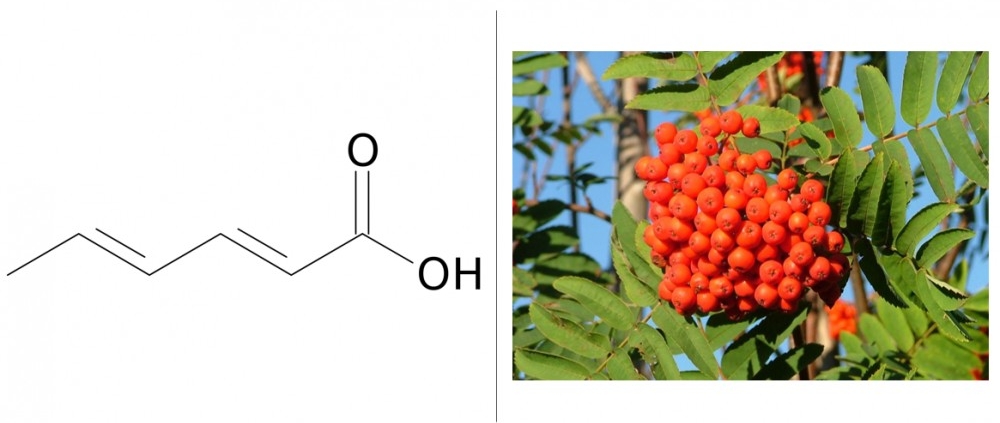
L’acide sorbique : que cache donc ce conservateur issu du sorbier ?
Les conservateurs sont des ingrédients cosmétiques extrêmement critiqués. Ils sont la cible préférée des consommateurs mais sont pourtant indispensables si l’on veut préserver la qualité microbiologique du milieu. L’origine végétale de l’acide sorbique plaide en sa faveur, à une époque où l’on est persuadé que tout ce qui est naturel est parfaitement sain. Des baies de sorbier au sorbet cosmétique hydratant,1 en passant par le vin ou les fruits secs, nous nous proposons de faire sauter le vernis qui recouvre cet ingrédient et d’en apprendre plus sur l’additif alimentaire E200.
L’acide sorbique, un conservateur antimicrobien naturel
La baie de cendre de montagne ou baie de sorbier (Sorbus aucuparia) a la réputation d’améliorer la résistance des conserves de fruits rouges aux attaques microbiennes. Certains auteurs font de l’ironie à son sujet, en constatant que, sur des baies séchées à l’air libre, on peut retrouver, tout de même, une grande variété de micro-organismes. Ceux-ci n’hésitent pas à mettre à mal les théories de nos grand-mères. Si l’on creuse un peu plus, on se rend compte que les baies de sorbier contiennent une lactone, l’acide parasorbique,2 qui exerce un rôle fongistatique et inhibiteur de la germination des graines.3 Par hydrolyse acide, l’acide parasorbique est transformé en acide sorbique.4 Les propriétés antimicrobiennes de l’acide sorbique ou acide 2,4 hexanediénoïque5 ont été démontrées pour la première fois dans les années 19306 et exploitées dans le domaine alimentaire une dizaine d’années plus tard.7
L’acide sorbique (E200) et ses sels, le sorbate de potassium (E202), en particulier, sont des conservateurs antimicrobiens très utilisés dans le domaine agro-alimentaire. Ces conservateurs permettent d’inhiber la croissance d’un certain nombre de bactéries Gram positif ou Gram négatif, catalase positif ou catalase négatif, aérobies et anaérobies, thermophiles, mésophiles et psychotrophes, mais également de levures et de moisissures. Les concentrations nécessaires pour inhiber la prolifération bactérienne dans les aliments dépendent de différents facteurs tels que l’activité de l’eau, la composition du produit (salé, sucré, épicé…), son pH, ses conditions de conservation… La dose nécessaire pour permettre l’inhibition de la croissance bactérienne varie de 10 à 10 000 ug/mL, sachant que les germes des genres Lactobacillus et Clostridium sont les moins sensibles. C’est à pH 6 que son efficacité est optimale.8
L’emploi d’acide sorbique comme agent conservateur n’est pas adapté à tout type d’aliment. Dans le vin, par exemple, les bactéries lactiques sont capables de transformer l’acide sorbique en alcool sorbique, responsable d’une odeur de géranium. Les olives vertes et la saumure dans laquelle elles sont plongées voient, quant à elles, leur couleur modifiée en présence d’acide sorbique.9
L’acide sorbique, un ingrédient aux qualités peu exploitées
La conservation de certains fruits secs nécessite l’emploi de conservateurs antimicrobiens lorsque le degré d’humidité résiduelle est jugé encore trop élevé. Dans ce cas, on peut avoir recours à l’acide sorbique. Celui-ci permet, en outre, de protéger de l’oxydation certaines molécules telles que les caroténoïdes par exemple.10
Dans le domaine médical, l’acide sorbique présente un intérêt en ophtalmologie car il permettrait une augmentation de la biodisponibilité de certains principes actifs tel que le timolol.11 En pratique, cette notion n’est pas exploitée à l’heure actuelle.
L’acide sorbique, différents sons de cloches en matière de tolérance
En matière de toxicité, nous sommes rassurées. Utilisé même à forte dose (5 – 10 %) et pendant de longues périodes (80 semaines) chez la souris, l’acide sorbique est très bien toléré et n’engendre aucune modification histologique.12 Même constat chez le rat soumis au même type de régime.13
En matière de tolérance, il est utile d’écouter les différents avis concernant cet ingrédient. Pour certains auteurs, l’acide sorbique est considéré comme un conservateur susceptible d’engendrer différents types de réactions telles qu’urticaire non immunologique,14,15 érythème, œdème, flush, picotements modérés et ce même pour une faible dose d’emploi (soit 0,1 %). Ces manifestations sont mises en relation avec la libération de prostaglandines, des molécules impliquées dans la réaction inflammatoire.16 Les médicaments et les cosmétiques qui en contiennent sont donc capables d’engendrer ce type de réactions et il faut y penser en cas d’effets indésirables survenant chez le patient. L’acide sorbique est également déconseillé pour la formulation des produits destinés au sujet atteint de rosacée.17 En 1985, une étude multicentrique réalisée aux Etats-Unis sur un échantillon de 281 100 patients fait état de réactions allergiques liées à l’utilisation d’un cosmétique dans 0,3 % des cas. Il n’est pas toujours aisé de déterminer la cause précise de l’allergie. Sur les 538 réactions allergiques pour lesquelles l’agent responsable a été identifié, on se rend compte que le parfum vient en tête de liste (dans 161 des cas répertoriés) et l’acide sorbique en queue de peloton (dans 6 des cas répertoriés).18 Un cas d’allergie au tabac liée à la présence d’acide sorbique dans ce dernier a également été publié dans la littérature en 2008 ; le patient avait été sensibilisé au préalable par des applications de Fucidine, une crème ayant un statut de médicament et dont le conservateur est l’acide sorbique.19 Dans ces conditions, l’acide sorbique est répertorié dans la liste des excipients à effet notoire devant être signalé aux patients. Il est présenté comme susceptible de « provoquer des réactions locales (exemple eczéma) ».20 La dermatologue Zoe Draelos classe également l’acide sorbique dans les conservateurs susceptibles d’engendrer des urticaires.21 Lorsque l’on réaliste un « stinging test » afin de savoir si un patient possède une peau réactive ou non on pourra utiliser de l’acide lactique, de la capsaïcine, de l’alcool, du menthol, de l’acide benzoïque ou de l’acide sorbique pour déclencher la réaction d’inconfort.22
En 2018, changement d’angle de vue. L’acide sorbique est alors considéré comme un conservateur bien toléré. Une étude visant à démontrer l’effet cicatrisant d’une crème composée de macrogol-20-glycerol monostearate, de glycerol mono/di (palmitate et stearate), d’octyldodécanol, d’isopropyl myristate, de propylène glycol, de diméticone 100, d’huile essentielle de romarin, d’acétate de tocopherol, d’acide citrique, d’eau purifiée, d’acide sorbique et de salicylate d’hydroxyéthyle et d’un extrait de consoude permet de mettre en avant les qualités de ce conservateur. Sur la cohorte de 700 enfants inclus dans l’étude, on ne constate qu’un seul cas d’effet indésirable avec rougeur et sensation de brûlure.23 Les auteurs n’ont pas cherché à savoir quel ingrédient était en cause.
Si l’on souhaite réaliser une crème émolliente à destination du sujet atopique, l’utilisation d’acide sorbique est envisageable. Le risque de développer une allergie est jugé, faible contrairement au risque lié à l’utilisation d’une préparation contenant un générateur de formol comme la diazolidinylurée, par exemple.24
L’acide sorbique, quelques incompatibilités à connaître
En solution aqueuse, l’acide sorbique et ses sels, les sorbates, sont capables de s’oxyder avec formation de composés carbonylés. On a pu penser qu’ajouter de l’EDTA dans la préparation pourrait être un moyen d’éviter ce phénomène. Il n’en est rien. Une étude datant de 1996 a montré que le complexe EDTA–Fe2+ favorise le phénomène d’oxydation et provoque un phénomène de brunissement.25 Un changement de couleur est également observé lorsque l’acide sorbique est associé à la vanilline ou à l’éthylvanilline ainsi qu’à des acides aminés.26 Il est donc important de réaliser des tests de stabilité et de vérifier que l’acide sorbique ne présente pas d’incompatibilité avec les autres ingrédients de la formule.
L’acide sorbique, en un mot
Les amateurs d’ingrédients naturels peuvent se rassurer. L’acide sorbique a peu de choses à cacher. Il ne simule pas la gentillesse. Il est vraiment gentil. On doit, toutefois, garder à l’esprit qu’il peut être mal toléré par les sujets à peau réactive et engendrer, dans de rares cas, des réactions allergiques. Les formulateurs devront être vigilants quant aux associations à réaliser, sous peine de voir « virer » la couleur du produit lors de son vieillissement.
Bibliographie
1 https://www.regard-sur-les-cosmetiques.fr/nos-regards/les-sorbets-cosmetiques-289/
3 J. H. Cardellina, J. Meinwald, Isolation of parasorbic acid from the cranberry plant, Vaccinium macrocarpon, Phytochemistry, 19, 10, 1980, Pages 2199-2200
4 P. L. Mason, I. F. Gaunt, J. Hardy, I. S. Kiss, S. D. Gangolli, Long-term toxicity of parasorbicacid in rats, Food and Cosmetics Toxicology, 14, 5, 1976, Pages 387-394
5 Giovanni Burini, Pietro Damiani, Determination of sorbicacid in margarine and butter by high-performance liquid chromatography with fluorescence detection, Journal of Chromatography A, 543, 1991, Pages 69-80
6 R. G. Bell, Karen M. De Lacy, The efficacy of nisin, sorbicacid and monolaurin as preservatives in pasteurized cured meat products, Food Microbiology, 4, 4, 1987, Pages 277-283
7 Seyedeh Homa Fasihnia, Seyed Hadi Peighambardoust, Seyed Jamaleddin Peighambardoust, Abdulrasoul Oromiehie, Development of novel active polypropylene based packaging films containing different concentrations of sorbicacid, Food Packaging and Shelf Life, 18, 2018, Pages 87-94
8 J. N. Sofos, M. D. Pierson, J. C. Blocher, F. F. Busta, Mode of action of sorbicacid on bacterial cells and spores, International Journal of Food Microbiology, 3, 1, 1986, Pages 1-17
9 Francisco Javier Casado, Antonio Higinio Sánchez, Luis Rejano, Antonio de Castro, Alfredo Montaño, Stability of sorbic and ascorbic acids in packed green table olives during long-term storage as affected by different packing conditions, and its influence on quality parameters, Food Chemistry, 122, 3, 2010, Pages 812-818
10 Sümeyye Alagöz, Meltem Türkyılmaz, œžeref Tağı, Mehmet Özkan, Effects of different sorbicacid and moisture levels on chemical and microbial qualities of sun-dried apricots during storage, Food Chemistry, 174, 2015, Pages 356-364
11 Masayo Higashiyama, Katsuhiro Inada, Akira Ohtori, Kakuji Tojo, Improvement of the ocular bioavailability of timolol by sorbicacid, International Journal of Pharmaceutics, 272, 1–2, 2004, Pages 91-98
12 R. J. Hendy, J. Hardy, I. F. Gaunt, I. S. Kiss, K. R. Butterworth, Long-term toxicity studies of sorbic acid in mice, Food and Cosmetics Toxicology, 14, 5, 1976, Pages 381-386
13 I. F. Gaunt, K. R. Butterworth, Joan Hardy, S. D. Gangolli, Long-term toxicity of sorbic acid in the rat, Food and Cosmetics Toxicology, 13, 1, 1975, Pages 31-45
14 Substances that affect the skin: Contact urticaria, Meyler’s Side Effects of Drugs (Sixteenth Edition), 2016, Pages 523-527
15 Peck Y. Ong, Mark Boguniewicz, Atopic Dermatitis and Contact Dermatitis in the Emergency Department, Clinical Pediatric Emergency Medicine, 8, 2, 2007, Pages 81-86) (J. Harvell, M. Bason, H. Maibach, Contact urticaria and its mechanisms, Food and Chemical Toxicology, 32, 2, 1994, Pages 103-112
16 Daniel S. VanderEnde, Jason D. Morrow, Release of markedly increased quantities of prostaglandin D2 from the skin in vivo in humans after the application of cinnamic aldehyde, Journal of the American Academy of Dermatology, 45, 1, 2001, Pages 62-67
17 Dora Soschin, James J. Leyden, Sorbicacid-induced erythema and edema, Journal of the American Academy of Dermatology, 14, 2, Part 1, 1986, Pages 234-241
18 Andrew Scheman, Adverse reactions to cosmetic ingredients, Dermatologic Clinics, 18, 4, 2000, pages 685 – 698.
19 A. Grange-Prunier, M. Bezier, G. Perceau, P. Bernard, Eczéma de contact au tabac par sensibilisation à l’acide sorbique, Annales de Dermatologie et de Vénéréologie, 135, 2, 2008, Pages 135-138
21 Zoe Diana Draelos, Facial skin care products and cosmetics, Clinics in Dermatology, 32, 6, 2014, Pages 809-812
22 J. Escalas-Taberner, E. González-Guerra, A. Guerra-Tapia, Sensitive Skin: A Complex Syndrome, Actas Dermo-Sifiliográficas (English Edition), 102, 8, 2011, Pages 563-571
23 Alexander Kucera, Milos Barna, Simona Holcova, Ondrej Horacek, Bertram Ottillinger, Tolerability and effectiveness of an antitrauma cream with comfrey herb extract in pediatric use with application on intact and on broken skin, International Journal of Pediatrics and Adolescent Medicine, In press, accepted manuscript, 2018
24 Marie Lodén, The skin barrier and use of moisturizers in atopic dermatitis, Clinics in Dermatology, 21, 2, 2003, Pages 145-157
25 Carmen A. Campos, Ana M. Rojas, Lía N. Gerschenson, Studies of the effect of ethylene diamine tetraacetic acid (EDTA) on sorbicacid degradation, Food Research International, 29, 3–4, 1996, Pages 259-264
26 C. C. Seow, P. B. Cheah, Kinetics of degradation of sorbicacid in aqueous glycerol solutions, Food Chemistry, 17, 2, 1985, Pages 95-103