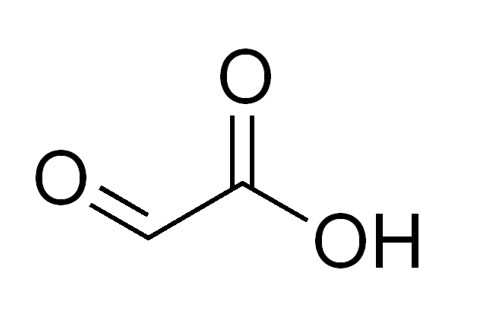
L’acide glyoxylique, comme un cheveu sur la soupe cosmétique !
L’acide glyoxylique est un acide susceptible d’être retrouvé dans le vin (il s’agit alors d’un produit de dégradation de l’acide tartrique).1,2 Cet acide est un acide susceptible de se former lors du traitement des eaux usées par ozonation.3 C’est aussi un polluant de l’air atmosphérique.4 Il peut donner naissance à du formaldéhyde par oxydation.5,6 C’est enfin un actif présent dans les « défrisants chimiques », présentés comme étant sans formol, donc sûrs pour la santé.7
L’acide glyoxylique est décidément un drôle de coco… qui s’invite dans nos verres et dans notre air (à petites doses) et dans nos cosmétiques dans des proportions variables (utilisé à des doses allant de 0,5 à 10 %).8
Un ingrédient dont on parle beaucoup en ce moment9 et qui méritait donc un Regard un peu appuyé de notre part !
Le cheveu, trois couches superposées
Le cheveu (ou le poil puisqu’il s’agit d’une seule et même structure) est une structure kératinisée, composée de l’empilement de trois couches distinctes qui sont, de l’intérieur vers l’extérieur, la moelle, le cortex, la cuticule (autrement dit la partie visible du cheveu). D’un point de vue chimique, ce cheveu est composé à 90 % de kératine et de lipides (1 à 9%).10,11 Cette kératine est caractérisée par sa richesse en cystéine, un acide aminé capable d’établir des liaisons particulières (appelées ponts disulfures) de manière inter- ou intra-chaîne,12 car il faut préciser que la kératine est formée par des filaments de kératine de types I et II.13
Le lissage des cheveux, les techniques à disposition
Lorsque l’on veut changer la nature de son cheveu (le rendre frisé, alors qu’il est lisse ou bien lisse, alors qu’il est frisé), on peut opter pour l’une ou l’autre de deux solutions. On pourra ainsi utiliser des ingrédients alcalins (à base d’hydroxydes de sodium, de potassium et de lithium, de carbonate de guanidine, de bisulfites et de thiols), qui provoquent la rupture entre les ponts disulfures qui stabilisent la kératine. Une fois ces « ponts » cassés, le cheveu devient malléable et on peut lui donner la forme souhaitée. Il faut, toutefois, utiliser dans un second temps, un cosmétique à pH acide qui permet au cheveu de conserver la forme que l’on vient de lui donner artificiellement, en reconstituant des ponts disulfures aux endroits voulus. Il s’agit donc de casser des liaisons existantes (celles dont on ne veut pas, car elles donnent au cheveu une forme non désirée), afin d’en construire de nouvelles (celles qui conviennent parfaitement car elles confèrent au cheveu l’aspect convoité) !
On peut aussi ne pas passer par la case « alcaline » et fonctionner de A à Z en pH acide. C’est le cas lorsque l’on a recours à l’acide glyoxylique ou à ses dérivés (glyoxyloyl carbocystéine, glyoxyloyl cystein, glyoxyloyl keratin amino acids…).14-16 Ces molécules à caractère acide sont à l’origine de modifications chimiques de la tige pilaire (formation d’hémithioacétals et d’imine).11 Lorsque l’on a recours à ces ingrédients, l’usage d’un fer à lisser est indispensable. Le chauffage à une température de 200°C est, semble-t-il, un facteur important d’un point de vue du mécanisme chimique en question. Cette température élevée permet la libération de formaldéhyde en quantité suffisante pour former avec la kératine du cheveu un biopolymère (polyacétal) doué de qualités indéniables et recherchées : la brillance, l’hydrophobie, la rigidité.17 Tiens, tiens… on nous disait, pourtant, que ce genre de produit de lissage était « sans formol ».18
L’acide glyoxylique au Cosing
Pour l’inventaire européen, l’acide glyoxylique est un ingrédient cosmétique bien anodin, connu sous le nom INCI glyoxylic acid et susceptible d’être retrouvé dans les produits capillaires, du fait de ses propriétés « antistatiques » et de son intérêt dans le cadre de la formulation de produits destinés à « l’ondulation ou au défrisage des cheveux ». Un effet « tampon » est également noté à l’inventaire européen pour cet ingrédient qui n’émarge dans aucune Annexe du Règlement (CE) N°1223/2009.19
L’acide glyoxylique, un drôle de « tampon »
Le lissage des cheveux à l’aide d’acide n’est pas chose rare. D’un point de vue pratique, on sait que plus le cosmétique possède un pH acide (mais vraiment acide, très acide, c’est-à-dire inférieur à 2 !!!), plus l’efficacité en matière de lissage est importante. Le revers de la médaille consiste en une fragilisation de la fibre capillaire, avec une résistance à la traction qui diminue d’autant plus que le pH lui-même diminue.20 Et puis, côté tolérance… évidemment ce pH n’est guère recommandable !
L’acide glyoxylique, une toxicité rénale démontrée
La toxicité rénale de l’acide glyoxylique vient d’être démontrée chez un patient (une jeune femme de 26 ans) ayant réalisé un lissage brésilien.21 Cette toxicité s’explique par le fait que l’acide glyoxylique, une fois absorbé par la peau, peut être métabolisé par l’organisme en oxalate, qui est néphrotoxique. Ceci a été démontré chez l’animal, à l’aide de crème contenant 10 % d’acides glyoxylique et glycolique.22 Il est intéressant de savoir que l’acide glycolique est présenté par des équipes de recherche japonaises comme l’ingrédient idéal pour optimiser l’action lissante de l’acide glyoxylique, du fait de son caractère exhausteur de pénétration dans la fibre capillaire.23
On peut ajouter que le métabolisme des acides glyoxylique et glycolique en oxalate est un fait connu depuis des années.24-30 Les intoxications aux produits antigel à base d’éthylène-glycol (qui se décompose en acide glyoxylique, puis en oxalate) produisent ce que l’on appelle une « oxalose » ou hyperoxalurie, nécessitant a minima une hémodialyse.31
L’acide glyoxylique, en bref
Cet ingrédient, inconnu du Règlement (CE) N°1223/2009, inconnu du CIR,32 mais trop bien connu de la littérature scientifique, mériterait qu’on lui fasse un sort rapidement, avant qu’il ne fasse trop de victimes. Et tant qu’à faire on pourrait se pencher aussi sur le cas de l’acide glycolique,33 en particulier et sur les acides de fruit, en général, afin de cadrer leur utilisation. On pourrait également s’intéresser de manière active à tous ces générateurs de formol,34 qui libèrent, en douce, une substance heureusement désormais interdite dans un produit qui doit, en théorie, être parfaitement sûr d’emploi…
Bibliographie
1 Grant-Preece P, Schmidtke LM, Barril C, Clark AC. Photoproduction of glyoxylic acid in model wine: Impact of sulfur dioxide, caffeic acid, pH and temperature. Food Chem. 2017 Jan 15;215:292-300
2 Castro Marin A, Stocker P, Chinnici F, Cassien M, Thétiot-Laurent S, Vidal N, Riponi C, Robillard B, Culcasi M, Pietri S. Inhibitory effect of fungoid chitosan in the generation of aldehydes relevant to photooxidative decay in a sulphite-free white wine. Food Chem. 2021 Jul 15;350:129222
3 Manasfi T, Houska J, Gebhardt I, von Gunten U. Formation of carbonyl compounds during ozonation of lake water and wastewater: Development of a non-target screening method and quantification of target compounds. Water Res. 2023 Jun 15;237:119751
4 Röhrl A, Lammel G. Low-molecular weight dicarboxylic acids and glyoxylic acid: seasonal and air mass characteristics. Environ Sci Technol. 2001 Jan 1;35(1):95-101
5 Deng Y, Englehardt JD, Abdul-Aziz S, Bataille T, Cueto J, De Leon O, Wright ME, Gardinali P, Narayanan A, Polar J, Tomoyuki S. Ambient iron-mediated aeration (IMA) for water reuse. Water Res. 2013 Feb 1;47(2):850-8
6 Fearon WR. A Study of some Biochemical Tests. No. 2: The Adamkiewicz Protein Reaction. The Mechanism of the Hopkins-Cole Test for Tryptophan. A New Colour Test for Glyoxylic Acid. Biochem J. 1920 Oct;14(5):548-64
7 Abu-Amer N, Silberstein N, Kunin M, Mini S, Beckerman P. Acute Kidney Injury following Exposure to Formaldehyde-Free Hair-Straightening Products. Case Rep Nephrol Dial. 2022 Jul 11;12(2):112-116
9 https://anses.fr/fr/content/actu-lissage
10 Hatsbach de Paula JN, Basílio FMA, Mulinari-Brenner FA. Effects of chemical straighteners on the hair shaft and scalp. An Bras Dermatol. 2022 Mar-Apr;97(2):193-203
11 Boga C, Taddei P, Micheletti G, Ascari F, Ballarin B, Morigi M, Galli S. Formaldehyde replacement with glyoxylic acid in semipermanent hair straightening: a new and multidisciplinary investigation. Int J Cosmet Sci. 2014 Oct;36(5):459-70
12 Ye W, Qin M, Qiu R, Li J. Keratin-based wound dressings: From waste to wealth. Int J Biol Macromol. 2022 Jun 30;211:183-197
13 Rogers MA, Winter H, Langbein L, Wollschläger A, Praetzel-Wunder S, Jave-Suarez LF, Schweizer J. Characterization of human KAP24.1, a cuticular hair keratin-associated protein with unusual amino-acid composition and repeat structure. J Invest Dermatol. 2007 May;127(5):1197-204
14 https://ec.europa.eu/growth/tools-databases/cosing/details/88884
15 https://ec.europa.eu/growth/tools-databases/cosing/details/94506
16 https://ec.europa.eu/growth/tools-databases/cosing/details/88858
17 Velasco MVR, de Sá-Dias TC, Dario MF, Bedin V, Fileto MB, de Oliveira AC, Pinto CASO, Baby AR. Impact of Acid (« Progressive Brush ») and Alkaline Straightening on the Hair Fiber: Differential Effects on the Cuticle and Cortex Properties. Int J Trichology. 2022 Nov-Dec;14(6):197-203
18 https://sklbeauty.com/products/lissages-bresiliens-100-ml-sans-formol
19 https://ec.europa.eu/growth/tools-databases/cosing/details/34158
20 Goshiyama AM, Dario MF, Lima CRRC, de Araújo GLB, Baby AR, Velasco MVR. Impact of acid straightener’s pH value in the hair fiber properties. J Cosmet Dermatol. 2020 Feb;19(2):508-513
21 Robert T, Tang E, Kervadec J, Zaworski J, Daudon M, Letavernier E. Kidney Injury and Hair-Straightening Products Containing Glyoxylic Acid. N Engl J Med. 2024 Mar 21;390(12):1147-1149
22 Robert T, Tang E, Kervadec J, Desmons A, Hautem JY, Zaworski J, Daudon M, Letavernier E. Hair-straightening cosmetics containing glyoxylic acid induce crystalline nephropathy. Kidney Int. 2024 Aug 26:S0085-2538(24)00619-7
23 Uyama M, Okabe S, Kurashima T, Kurinobu R, Takechi M, Yoshiba R, Miyoshi R, Noda S, Kaneko M, Ikemoto Y, Takahara A, Higaki Y, Hama T. Promotion of glyoxylic acid penetration into human hair by glycolic acid. Int J Cosmet Sci. 2023 Apr;45(2):246-254
24 Leth PM, Gregersen M. Ethylene glycol poisoning. Forensic Sci Int. 2005 Dec 20;155(2-3):179-84
25 Brent J. Current management of ethylene glycol poisoning. Drugs. 2001;61(7):979-88
26 Corley RA, Saghir SA, Bartels MJ, Hansen SC, Creim J, McMartin KE, Snellings WM. Extension of a PBPK model for ethylene glycol and glycolic acid to include the competitive formation and clearance of metabolites associated with kidney toxicity in rats and humans. Toxicol Appl Pharmacol. 2011 Feb 1;250(3):229-44
27 Guo C, Cenac TA, Li Y, McMartin KE. Calcium oxalate, and not other metabolites, is responsible for the renal toxicity of ethylene glycol. Toxicol Lett. 2007 Aug 30;173(1):8-16
28 Veena CK, Josephine A, Preetha SP, Varalakshmi P. Effect of sulphated polysaccharides on erythrocyte changes due to oxidative and nitrosative stress in experimental hyperoxaluria. Hum Exp Toxicol. 2007 Dec;26(12):923-32
29 Bringmann G, Feineis D, Hesselmann C, Schneider S, Koob M, Henschler D. A « chemical » concept for the therapy of glyoxylate-induced oxalurias (1). Life Sci. 1992;50(21):1597-605
30 Ovrebø S, Jacobsen D, Sejersted OM. Determination of ionic metabolites from ethylene glycol in human blood by isotachophoresis. J Chromatogr. 1987 Apr 24;416(1):111-7
31 Samarneh MM, Shtaynberg N, Goldman M, Epstein E, Kleiner M, El-Sayegh S. Severe oxalosis with systemic manifestations. J Clin Med Res. 2012 Feb;4(1):56-60
32 https://www.cir-safety.org/